|
Getting your Trinity Audio player ready...
|
Importancia de las Hormonas Tiroideas
- Desarrollo y Homeostasis: Las hormonas tiroideas son cruciales para el desarrollo normal, particularmente del Sistema Nervioso Central (SNC). En adultos, son fundamentales para mantener la homeostasis metabólica e influyen en las funciones de casi todos los órganos y sistemas.
- Contenido de Yodo: Estas hormonas contienen yodo, elemento que debe ser adquirido a través de la dieta.
- Almacenamiento en la Glándula Tiroides: La glándula tiroides alberga grandes reservas de hormonas tiroideas en forma de tiroglobulina, lo que asegura niveles adecuados en el sistema a pesar de las variaciones en la disponibilidad de yodo y la ingesta dietética.
- Secreción y Conversión: La secreción tiroidea se realiza principalmente en forma de T4 (prohormona), que se transforma en el hígado y otros tejidos en T3 (forma activa), tanto en el plasma como en los tejidos diana, como el cerebro y la hipófisis. La activación y desactivación locales de T4 a T3 son pasos reguladores críticos.
- Regulación por TSH: Las concentraciones de hormonas tiroideas en el suero son reguladas por la TSH hipofisaria, mediante un sistema de retroalimentación negativa. La acción de las hormonas tiroideas está mediada por receptores nucleares que afectan la transcripción de genes específicos.
Trastornos Tiroideos y su Tratamiento
- Hipertiroidismo e Hipotiroidismo: El exceso (hipertiroidismo) y la deficiencia (hipotiroidismo) de hormonas tiroideas conllevan numerosas manifestaciones clínicas. Las formas leves pueden tener síntomas sutiles y detectarse solo por pruebas bioquímicas anormales.
- Hipotiroidismo Materno y Neonatal: La deficiencia de yodo es una causa principal prevenible de discapacidad intelectual a nivel mundial. El tratamiento del hipotiroidismo implica la sustitución de hormonas tiroideas.
- Tratamientos del Hipertiroidismo: Incluyen medicamentos antitiroideos, destrucción de la glándula tiroides con yodo radiactivo, y extirpación quirúrgica. La mayoría de los trastornos de la función tiroidea son tratables o controlables.
Neoplasias Tiroideas
- Resección y Tratamiento: Las neoplasias tiroideas generalmente son localizadas y susceptibles a la resección quirúrgica. La enfermedad metastásica responde al tratamiento con yodo radiactivo, aunque puede volverse agresiva. Los cánceres de tiroides avanzados y resistentes al yodo radiactivo pueden tratarse con quimioterapias dirigidas, como los inhibidores de la tirosina cinasa.
Tipos de Hormonas Producidas por la Glándula Tiroides
Hormonas Tiroideas T4 y T3
- Producción por el Folículo Tiroideo: Las hormonas T4 (tiroxina) y T3 (triyodotironina) son producidas por los folículos tiroideos a partir de tirosina yodada. Estas hormonas son esenciales para numerosas funciones metabólicas y el desarrollo normal.
Calcitonina
- Producción por Células Parafoliculares: La calcitonina es un péptido de 32 aminoácidos producido por las células parafoliculares (o células C) del tiroides. A diferencia de T4 y T3, la calcitonina no juega un papel endógeno significativo en el metabolismo general.
- Uso Terapéutico: Aunque no es crucial como las hormonas tiroideas T4 y T3 para el metabolismo diario, la calcitonina puede ser útil como tratamiento para condiciones específicas como la hipercalcemia (niveles elevados de calcio en la sangre) y la osteoporosis, ayudando a reducir los niveles de calcio en la sangre y potencialmente a mejorar la salud ósea.
Química de las Hormonas Tiroideas
Componentes Principales
- Aminoácidos Derivados de la Tironina: Las hormonas principales de la glándula tiroides son aminoácidos que derivan de la tironina y contienen yodo.
Descubrimiento y Actividad Hormonal
- Enfoque Inicial en T4: Inicialmente, se pensaba que la tiroxina (T4) era responsable de toda la actividad hormonal del tejido tiroideo, basándose en su aislamiento e identificación química.
- Mayor Actividad Calorígena Observada: Investigaciones posteriores mostraron que extractos crudos de la glándula tiroides tenían más actividad metabólica de lo que la T4 sola podía explicar, sugiriendo la existencia de otra hormona tiroidea.
Descubrimiento de T3
- Identificación de T3: La hipótesis de una “segunda” hormona tiroidea llevó a Gross y Pitt-Rivers a descubrir, aislar y sintetizar la triyodotironina (T3) en 1952.
- Mayor Potencia de T3: Se encontró que la T3 tiene una mayor afinidad por los receptores nucleares de hormonas tiroideas y es biológicamente más potente que la T4 en una base molar.
Implicaciones Clínicas
- Conversión de T4 a T3: Se demostró posteriormente que la T3 se produce a partir de T4 en humanos sin tiroides, lo que llevó a la práctica de tratar el hipotiroidismo eficazmente con solo levotiroxina (una forma de T4), aprovechando la capacidad del cuerpo para convertir T4 en T3.
Biosíntesis de las Hormonas Tiroideas
Síntesis y Almacenamiento
- Tiroglobulina como Precursor: Las hormonas tiroideas se sintetizan y almacenan unidas a la tiroglobulina, una glucoproteína compleja que se compone de dos subunidades que parecen idénticas. Esta proteína es la principal constituyente del coloide dentro de los folículos tiroideos.
- Capacidad de Almacenamiento Única de la Tiroides: La glándula tiroides es única en su capacidad para almacenar grandes cantidades de estos precursores hormonales, siendo la cantidad de tiroglobulina extracelular proporcional al tamaño de la glándula tiroides.
Proceso de Producción Hormonal
- Pasos Clave: Los procesos involucrados en la producción de hormonas tiroideas incluyen su síntesis a partir de la tiroglobulina, el almacenamiento de precursores hormonales, la liberación de hormonas activas y la conversión entre diferentes formas de hormonas tiroideas.
Vamos a imaginar que tu cuerpo es un restaurante que se especializa en hacer una pizza muy única: la pizza de hormonas tiroideas. Esta pizza tiene ingredientes especiales y un proceso de preparación único que asegura que todo en tu cuerpo funcione correctamente.
Ingredientes y Preparación de la Pizza de Hormonas Tiroideas
Ingredientes Básicos
- Tiroglobulina (Tg): Piensa en la tiroglobulina como la masa de pizza. Es la base sobre la que se construye todo.
- Yoduro (a través del NIS): El yoduro es como la salsa de tomate. El cotransportador unidireccional de yoduro de sodio (NIS) es el repartidor que trae el yoduro del exterior al interior de la glándula tiroides (la cocina del restaurante).
- Ácido Hipoyodoso (HOI) y Molécula Ligada a la Enzima (EOI): Estos son como los condimentos especiales que se agregan a la masa y la salsa para darle el sabor único de nuestra pizza. La peroxidasa tiroidea (TPO) ayuda a convertir el yoduro en estos ingredientes activos.
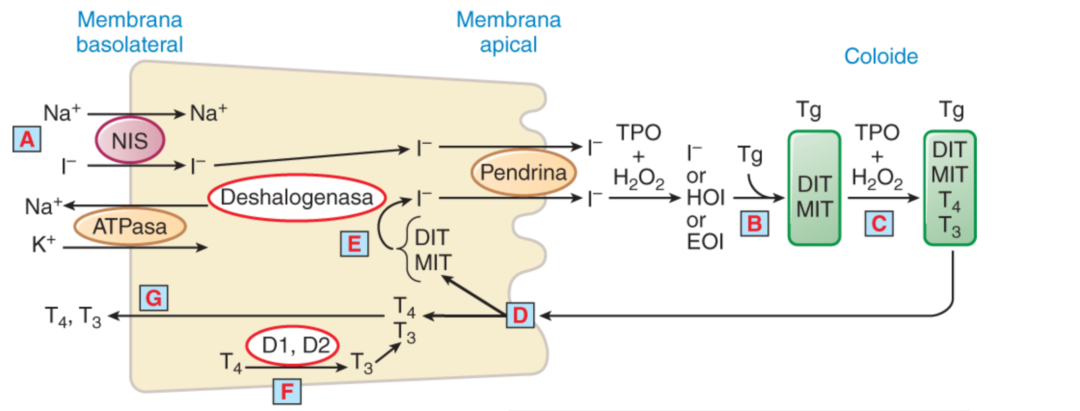
Preparando la Masa
- Diyodotirosina (DIT) y Monoyodotirosina (MIT): Una vez que la masa (Tg) está preparada con la salsa (yoduro) y los condimentos (HOI y EOI), agregamos los toppings: DIT y MIT. Estos son como los pepperonis y champiñones en nuestra pizza, esenciales para el sabor final.
Cocinando la Pizza
- Almacenamiento como Coloide: Antes de hornearla, nuestra pizza se deja reposar un poco en el coloide, que es como dejar la pizza en reposo para que los sabores se mezclen bien.
- Liberación: Cuando es hora de servir la pizza a todo el cuerpo, la pizza se “hornea” y se “sirve” en forma de hormonas T4 y T3, listas para ser distribuidas por todo el restaurante (tu cuerpo).
Interrupciones en la Cocina
- MMI (Metimazol) y PTU (Propiltiouracilo): Imagina que estos son como inspectores de salud que pueden ralentizar o detener la preparación de la pizza al interferir con los condimentos (bloqueando la TPO) o al evitar que los ingredientes se mezclen correctamente.
- SCN (Tiocianato): Es como otro inspector de salud que compite con el repartidor de salsa de tomate (NIS), dificultando la entrega de yoduro a la cocina.
Refinando el Sabor
- Desyodasas (D1, D2, D3): Estos son como los chefs de repostería que ajustan el sabor de la pizza después de hornearla, asegurándose de que la proporción de T4 a T3 sea perfecta para el paladar de quien la va a comer.
Captación de Yoduro en la Tiroides
¿Qué es el Yoduro?
- Yoduro en la Dieta: El yodo que comemos se transforma en ion yoduro (I−) en nuestro cuerpo y circula en la sangre. Normalmente, hay muy poco yoduro en nuestra sangre (0.2 a 0.4 mcg/100 mL).
¿Cómo la Tiroides Obtiene el Yoduro?
- Transporte Activo: La glándula tiroides usa una proteína especial en su superficie llamada cotransportador unidireccional de yoduro de sodio (NIS) para “absorber” activamente el yoduro de la sangre y llevarlo al interior de la tiroides.
- Concentración en la Tiroides: La tiroides puede acumular yoduro mucho más de lo que hay en la sangre. Cuando la tiroides está activa, puede aumentar aún más esta capacidad.
Factores que Afectan la Captación de Yoduro
- Inhibición por Iones: Algunos elementos, como el tiocianato y el perclorato, pueden bloquear o disminuir la capacidad de la tiroides para absorber yoduro.
- Estimulación por TSH: La hormona estimulante de la tiroides (TSH) puede aumentar la captación de yoduro al estimular la actividad y presencia del NIS en la membrana de la tiroides.
- Efecto del Yoduro Administrado: Dar yoduro como tratamiento puede, paradójicamente, disminuir la captación de yoduro por la tiroides al reducir la actividad del NIS.
Acumulación de Yoduro en Otros Tejidos
- Más Allá de la Tiroides: El yoduro también se acumula en otros tejidos del cuerpo, como las glándulas salivales, el intestino y las mamas durante la lactancia, gracias al gen NIS.
- Mutaciones del Gen NIS: Las personas con mutaciones en este gen pueden tener problemas para concentrar yoduro en estos tejidos, afectando la función tiroidea y otros procesos.
Oxidación y Yodación: Preparando el Yodo
Moviendo el Yodo
- De Célula a Almacén: El yodo se mueve desde las células de la tiroides hacia un espacio de almacenamiento llamado coloide. Esto lo hace un transportador especial llamado pendrina.
Activando el Yodo
- Encendiendo el Motor: La peroxidasa tiroidea es como un motor que enciende el yodo, transformándolo de su forma simple (yoduro) a una forma activa. Este paso se llama oxidación.
Creando Ingredientes Especiales
- MIT y DIT: Una vez activado, el yodo se une a la tiroglobulina (como una gran proteína almacenadora) formando MIT (monoyodotirosina) y DIT (diyodotirosina). Este proceso se llama organificación del yodo y es como preparar los ingredientes antes de guardarlos para su uso futuro.
Haciendo Hormonas Tiroideas: T4 y T3
Juntando las Piezas
- Construyendo T4 y T3: Ahora, imagina que MIT y DIT son piezas de LEGO. Para hacer T4, se juntan dos piezas DIT. Para hacer T3, se combina una pieza MIT con una DIT. La peroxidasa tiroidea nuevamente ayuda en este proceso, actuando como las manos que juntan los LEGOs.
El Toque Final
- De T4 a T3: Algunas T4 pueden transformarse en T3 dentro de la tiroides o después de ser secretadas. Esto es como modificar un LEGO ya construido para hacer un modelo ligeramente diferente. Este cambio se llama 5′-desyodación.
Síntesis y Secreción de Hormonas Tiroideas
Creación y Almacenamiento
- Tiroglobulina como Almacén: Tanto T4 como T3 se forman y guardan dentro de una sustancia llamada tiroglobulina, que es como una gran caja de almacenamiento para estas hormonas antes de que sean necesitadas.
Comenzando el Proceso de Liberación
- Endocitosis: La liberación de las hormonas comienza con un proceso llamado endocitosis, donde la tiroglobulina, que contiene las hormonas, es “ingerida” por la célula a través de su membrana.
- Participación de Megalina: Un receptor llamado megalina ayuda a que la tiroglobulina entre en la célula, capturándola para que pueda ser procesada.
Procesamiento Interno
- Fusión con Lisosomas: Una vez dentro, la tiroglobulina se encuentra con los lisosomas, que son como estaciones de procesamiento llenas de enzimas que cortan la tiroglobulina en partes más pequeñas.
- Rol de la TSH: La hormona estimulante de la tiroides (TSH) hace que este proceso de cortar la tiroglobulina sea más eficiente, activando las enzimas que se encargan de este trabajo.
Liberación de Hormonas
- Liberación de T4 y T3: Después de ser procesada, las hormonas son liberadas de la célula, principalmente como T4 y en menor cantidad como T3.
- Origen de la T3: La T3 que se libera proviene de dos fuentes: una parte ya está formada dentro de la tiroglobulina antes de ser procesada, y otra parte se forma transformando la T4 en T3, un proceso que también puede ocurrir fuera de la tiroides, en otros tejidos del cuerpo.
Metabolismo de la Hormona Tiroidea: Un Vistazo Cuantitativo
Diferencias entre T4 y T3
- Disponibilidad: La cantidad de T4 y T3 que circula libremente (sin unirse a proteínas) en la sangre es diferente. T4 se une más fuertemente a la proteína transportadora (TBG) que T3, lo que significa que hay menos T4 libre comparada con T3 libre.
Activación e Inactivación de la Hormona Tiroidea
Transformación de T4 en T3
- Importancia de la Desyodación: La mayoría de la T3 en nuestra sangre se forma al cambiar un átomo de yodo en la T4, principalmente en tejidos fuera de la tiroides. Este proceso se llama desyodación 5′ del anillo externo y es responsable de casi el 80% de la T3 circulante.
Creación de T3 Inversa
- T3 Inversa: Al modificar un átomo de yodo diferente en la T4, se produce una forma inactiva llamada T3 inversa (rT3).
Enzimas Clave en la Transformación de T4 en T3
Desyodasas: Los Artesanos de la Hormona Tiroidea
- Dio1 y Dio2: Estas enzimas convierten T4 en T3. Dio1 se encuentra principalmente en el hígado y los riñones, y su actividad cambia con el estado tiroideo. Dio2, presente en el cerebro y otros tejidos, es crucial para proporcionar T3 localmente a los receptores de hormona tiroidea.
Regulación de Dio1 y Dio2
- Respuesta a Cambios Hormonales: La cantidad y actividad de estas enzimas se ajustan según si hay demasiada o muy poca hormona tiroidea, ayudando a mantener el equilibrio correcto de T3.
Polimorfismo de Dio2
- Variaciones Genéticas: Algunas personas tienen una variante de Dio2 que reduce su actividad enzimática. Esto puede estar relacionado con diferencias en el peso corporal, la resistencia a la insulina, y cómo se sienten los pacientes hipotiroideos tratados con hormona tiroidea.
Inactivación de T3
Dio3: El Guardián de la Actividad Hormonal
- Controlando la T3: Dio3 convierte la T3 en una forma inactiva, regulando así las concentraciones de T3 activa, especialmente en el cerebro y durante el desarrollo.
Importancia de la Selenocisteína
Un Componente Especial de las Desyodasas
- Selenocisteína en las Desyodasas: Este aminoácido raro es crucial para la actividad de las enzimas desyodasas, y su incorporación en las enzimas es un proceso complejo.
Transporte de Hormonas Tiroideas en la Sangre
Distribución del Yodo y Hormonas Tiroideas
- Yodo en la Sangre: La mayoría del yodo en nuestra sangre (95%) es yodo orgánico, y un pequeño porcentaje (casi 5%) es yoduro. La T4 constituye la mayor parte del yodo orgánico (90% a 95%), mientras que la T3 solo representa una fracción menor (casi 5%).
Proteínas Transportadoras de Hormonas Tiroideas
- Globulina Transportadora de Tiroxina (TBG): Es la principal proteína responsable del transporte de las hormonas tiroideas, uniendo T4 con alta afinidad y T3 con menos afinidad.
- Transtiretina: Otra proteína importante que transporta principalmente T4. Aunque tiene menos afinidad que TBG, está presente en mayor concentración.
- Albúmina: Puede unirse a T4 bajo ciertas condiciones, pero su papel fisiológico no está claro.
Función de las Proteínas Transportadoras
- Protección y Vida Útil de las Hormonas: La unión de T4 y T3 a estas proteínas evita su rápido metabolismo y excreción, lo que resulta en una larga vida útil en la sangre.
- Porcentaje de Hormona Libre: Solo una pequeña fracción de las hormonas tiroideas circula libre sin unirse a proteínas (0.02% de T4 y 0.3% de T3), y solo esta fracción libre es metabólicamente activa.
Importancia de la Hormona Libre
- Actividad Metabólica: La capacidad de las hormonas tiroideas para influir en el metabolismo depende de su estado libre, es decir, no unido a proteínas transportadoras.
Influencia de Factores Externos
- Efectos de Fármacos y Condiciones de Salud: Tanto los medicamentos como los estados patológicos y fisiológicos pueden alterar cómo las hormonas tiroideas se unen a las proteínas plasmáticas y, por lo tanto, afectar las concentraciones totales de hormonas en el suero.
Degradación y Excreción de las Hormonas Tiroideas
Métodos de Metabolismo de T3 y T4
- Desyodación y Más: Tanto T3 como T4 pueden ser descompuestas mediante varios procesos: desyodación (retirar yodo), división del grupo funcional éter, conjugación con otras moléculas, y descarboxilación oxidativa, que es la eliminación de un grupo carboxilo con la adición de oxígeno.
Tiempo de Eliminación de T4
- Vida Media de T4: La T4 tarda bastante en ser eliminada del cuerpo, teniendo una vida media (t1/2) de 6 a 8 días bajo condiciones normales.
- Influencia del Estado Tiroideo:
- En el hipertiroidismo (tiroides hiperactiva), la vida media de T4 disminuye a 3 o 4 días.
- En el hipotiroidismo (tiroides poco activa), la vida media se extiende a 9 a 10 días.
- Impacto del Embarazo y Medicamentos:
- Durante el embarazo, la eliminación de T4 se retrasa debido al aumento de la unión a TBG (globulina transportadora de tiroxina).
- Algunos fármacos que inhiben la unión a proteínas pueden acelerar la eliminación de T4.
Tiempo de Eliminación de T3
- Vida Media de T3: La T3, que se une con menos fuerza a las proteínas transportadoras, tiene una vida media más corta, de aproximadamente 18 a 24 horas.
Regulación de la Secreción de la Hormona Tiroidea
Hormona Estimulante de la Tiroides (TSH)
- Estructura de la TSH: Es una hormona glucoproteica compuesta por dos subunidades: una subunidad α, que es común a otras glucoproteínas hipofisarias como las gonadotropinas, y una subunidad β única que le confiere especificidad.
- Secreción de la TSH: Se secreta de manera pulsátil y sigue un patrón circadiano, es decir, tiene variaciones a lo largo del día, con niveles ligeramente más altos durante el sueño nocturno.
Influencia del Cortisol
- Relación con el Cortisol: La secreción de TSH muestra un patrón inverso al del cortisol, indicando que el cortisol reduce la secreción de TSH.
Control Hipotalámico y Retroalimentación Negativa
- Regulación por TRH: La secreción de TSH es estimulada por el TRH (hormona liberadora de tirotropina), un péptido producido por el hipotálamo.
- Efecto de las Hormonas Tiroideas: Las hormonas tiroideas libres en circulación inhiben la producción de TSH al suprimir la transcripción del gen TRH y de los genes para las subunidades α y β de la TSH. Esto disminuye la secreción de TSH, llevando a una menor actividad de la tiroides.
Respuesta a Cambios en la Secreción de Hormonas Tiroideas
- Disminución en Hormonas Tiroideas: Una reducción en la secreción normal de hormonas tiroideas por la tiroides resulta en un aumento de la secreción de TSH.
- Mecanismos Adicionales:
- La hormona tiroidea también puede afectar la secreción de TSH reduciendo la liberación de TRH por el hipotálamo.
- Además, puede disminuir la cantidad de receptores de TRH en las células hipofisarias.
Hormona Liberadora de Tirotropina (TRH)
Estimulación de la TSH
- Función Principal: La TRH estimula la liberación de TSH almacenada en los gránulos secretores de la pituitaria y promueve la síntesis de las subunidades α y β de la TSH.
- Origen y Estructura: Es un tripéptido sintetizado por el hipotálamo y liberado en la circulación que conecta el hipotálamo con la pituitaria (circulación porta hipofisaria).
- Mecanismo de Acción: Al interactuar con los receptores en las células tirotropas de la pituitaria, la TRH activa una cadena de señalización intracelular que resulta en la síntesis y liberación de TSH.
Influencias Inhibitorias
- Regulación Negativa: Sustancias como la somatostatina, la dopamina y los glucocorticoides pueden inhibir la secreción de TSH estimulada por la TRH.
Acciones de la TSH en el Tiroides
Estímulo para la Producción de Hormonas
- Efectos de la TSH: Aumenta la síntesis y secreción de hormonas tiroideas al unirse a su receptor específico en las células tiroideas.
- Vías de Señalización: La unión de TSH a su receptor activa diferentes vías de señalización que facilitan la producción de hormonas tiroideas.
Mutaciones del Receptor de TSH
- Consecuencias de Mutaciones: Las mutaciones en el receptor de TSH pueden causar disfunciones tiroideas, incluyendo hipo o hipertiroidismo.
El Yodo y la Función Tiroidea
Importancia del Yodo
- Necesidad de Yodo: Es crucial para la síntesis normal de hormonas tiroideas. La deficiencia o el exceso de yodo pueden tener impactos significativos en la función tiroidea.
Efectos de la Deficiencia de Yodo
- Consecuencias de la Falta de Yodo: Puede resultar en producción reducida de hormonas tiroideas, aumento de la TSH, y cambios físicos en el tiroides como hiperplasia e hipertrofia.
Suplementación de Yodo
- Prevención de Deficiencias: La adición de yodato a la sal de mesa es un método eficaz para asegurar una ingesta adecuada de yodo.
- Recomendaciones de Consumo: Se establecen cantidades diarias recomendadas de yodo para diferentes grupos demográficos, incluyendo niños, adultos, embarazadas y lactantes.
- Las cantidades diarias recomendadas de yodo son de 90 a 120 mcg para los niños, 150 mcg para los adultos, 220 mcg para el embarazo y 290 mcg para la lactancia.
Fuentes Alimenticias de Yodo
- Variedad en la Dieta: Los productos lácteos y el pescado son ricos en yodo, mientras que las verduras, la carne y las aves contienen menos.
Transporte de Hormonas Tiroideas Dentro y Fuera de las Células
Transportadores Específicos
- Función: Facilitan el paso de las hormonas tiroideas a través de la membrana celular.
- Principales Transportadores: MCT8, MCT10, OATP1C1, y SLC17A4, con MCT8 siendo el más documentado.
Síndrome de Allan-Herndon-Dudley
- Causa: Mutaciones en MCT8.
- Consecuencias: Defectos graves del neurodesarrollo y alteraciones en los niveles de hormonas tiroideas circulantes.
Otras Vías de Transporte
- OATP1C1: Importante para el transporte de T4 en el cerebro.
- MCT10 y SLC17A4: Transportan T3 y T4 pero su importancia específica en humanos aún no está totalmente definida.
Mediación de los Efectos por los Receptores Nucleares
Unión de T3 a Receptores Nucleares
- Estructura de los Receptores: Tienen dominios específicos para unirse al ADN y al ligando (T3).
- Acción de T3 vs. T4: T3 se une con mayor afinidad a los receptores, siendo la principal hormona activa.
Genes de los Receptores de Hormonas Tiroideas
- THRA y THRB: Codifican para los receptores TRα1 y TRβ1/TRβ2 respectivamente, con roles específicos en distintos tejidos.
Mutaciones en Receptores
- Consecuencias: Pueden causar síndromes de resistencia a la hormona tiroidea, afectando distintas funciones corporales.
Efectos No Genómicos de la Hormona Tiroidea
Acciones Rápidas y No Genómicas
- Localización de Receptores: Fuera del núcleo, implicados en efectos biológicos rápidos y mecanismos no genómicos.
- Ejemplos de Acciones: Producción de NO dependiente de T3 y regulación de señales celulares como ERK y Akt.
Relevancia Fisiológica
- Estudios en Ratones: Muestran que la T3 puede regular funciones importantes como la frecuencia cardíaca y la temperatura corporal incluso cuando los receptores no pueden unirse al ADN.
- Posible Receptor en la Integrina αVβ3: Se une a T4 y podría estar involucrado en la activación de la MAP cinasa, aunque su importancia aún es incierta.
Efectos de la Hormona Tiroidea en Diversos Procesos Fisiológicos
Crecimiento y Desarrollo
- Metamorfosis de Anfibios: La T3 juega un papel crucial en la transformación de renacuajos en ranas, estimulando el desarrollo de extremidades y pulmones y la regresión de la cola.
- Desarrollo Cerebral: La hormona tiroidea es fundamental para el desarrollo cerebral. La deficiencia durante el periodo crítico de neurogénesis puede causar incapacidad intelectual irreversible y alteraciones morfológicas cerebrales. La suplementación temprana posnatal con hormonas tiroideas puede prevenir estos efectos.
- Hipotiroidismo Congénito: Puede ser endémico (por carencia de yodo) o esporádico, llevando a retraso del crecimiento, incapacidad intelectual y otros síntomas. El tratamiento temprano es crucial para evitar el desarrollo de estas condiciones.
Esqueleto
- Impacto en el Crecimiento: El hipotiroidismo infantil puede causar disminución del crecimiento lineal y anomalías óseas. Estos efectos están mediados en parte por el receptor TRα1.
Termogénesis
- Regulación del Calor: La hormona tiroidea es esencial tanto para la termogénesis obligatoria como para la facultativa, haciendo que los procesos biológicos sean menos eficientes para producir calor. Pequeños cambios en las dosis de hormona tiroidea pueden alterar significativamente el gasto energético.
Aparato Cardiovascular
- Efectos en el Corazón y Vasos Sanguíneos: El hipertiroidismo aumenta la tasa cardiaca y el volumen sistólico, mientras que el hipotiroidismo tiene efectos opuestos. La T3 regula la expresión génica miocárdica y tiene efectos inotrópicos y lusitrópicos en el corazón.
Metabolismo de los Lípidos
- Influencia en el Colesterol: La hormona tiroidea aumenta la expresión de receptores LDL hepáticos y reduce las concentraciones de apolipoproteína B, afectando así las concentraciones de colesterol en el cuerpo.
Mecanismos de Acción de la Hormona Tiroidea
- Receptores Nucleares: La T3 se une a receptores específicos en el núcleo de las células, induciendo o reprimiendo la transcripción de genes que regulan el crecimiento, el desarrollo y el metabolismo.
- Efectos No Genómicos: Además de sus efectos genómicos, la hormona tiroidea también puede actuar a través de mecanismos no genómicos rápidos, como la estimulación de la producción de NO y la activación de ciertas vías de señalización celular.
Trastornos de la Función Tiroidea
Hipofunción Tiroidea (Hipotiroidismo)
- Definición y Causas:
- El hipotiroidismo, conocido en su forma grave como mixedema, es el trastorno más común de la función tiroidea.
- La carencia de yodo es una causa común a nivel mundial, mientras que en zonas con suficiente yodo, la tiroiditis crónica autoinmunitaria (tiroiditis de Hashimoto) es la causa más frecuente.
- Se caracteriza por la presencia de anticuerpos contra la peroxidasa tiroidea y, a veces, contra la tiroglobulina.
- Tipos de Hipotiroidismo:
- Primario: Falla en la glándula tiroides.
- Secundario (Hipofisario): Falta de estimulación del tiroides por TSH debido a insuficiencia hipofisaria.
- Terciario (Hipotalámico): Insuficiencia hipotalámica que afecta la producción de TSH.
- Síntomas y Signos:
- Incluyen fatiga, intolerancia al frío, depresión, piel seca, estreñimiento, y bradicardia, entre otros.
- El hipotiroidismo congénito puede causar incapacidad intelectual si no se trata a tiempo.
Hiperfunción Tiroidea (Tirotoxicosis)
- Definición y Causas:
- La tirotoxicosis se debe a niveles elevados de hormonas tiroideas libres circulantes.
- La enfermedad de Graves es la causa más común, seguida por el bocio tóxico multinodular y la tiroiditis destructiva.
- Síntomas y Signos:
- Incluyen taquicardia, pérdida de peso, ansiedad, piel caliente y húmeda, y en casos graves, tormenta tiroidea.
- El hipertiroidismo subclínico se define por TSH baja con T4 y T3 libres normales.
Pruebas de Función Tiroidea
- Medición de Hormonas Tiroideas:
- La concentración total de hormonas tiroideas puede no reflejar con precisión la actividad tiroidea debido a variaciones en las proteínas transportadoras como TBG.
- Los análisis de T4 libre y T3 libre son más precisos pero están sujetos a interferencias por varios factores.
- Importancia de la TSH:
- La medición de TSH es la prueba preferida para evaluar la función tiroidea, ya que refleja las concentraciones circulantes de hormonas tiroideas y es sensible a cambios precoces en la función tiroidea.
Tratamiento con Hormonas Tiroideas: Levotiroxina y Liotironina
Levotiroxina (T4 Sintética)
- Química y Mecanismo de Acción: Imita a la hormona tiroidea natural T4.
- Absorción y Metabolismo: Se absorbe principalmente en el estómago e intestino delgado, con una absorción del 80% cuando se ingiere en ayunas. La vida media plasmática es de unos 7 días, permitiendo una administración diaria.
- Formulaciones: Disponible en comprimidos, cápsulas rellenas de líquido y polvo liofilizado para inyección.
- Dosis: La dosis intravenosa es aproximadamente el 80% de la dosis oral diaria.
Liotironina (T3 Sintética)
- Química y Mecanismo de Acción: Similar a la hormona tiroidea natural T3.
- Absorción y Metabolismo: Casi 100% absorbida, con niveles séricos máximos entre 2 y 4 horas después de la administración oral. La vida media plasmática es de casi 20 horas, requiriendo dosificación tres veces al día para mantener niveles estables.
Preparados Combinados de T4/T3
- Proporción: Mezclas de levotiroxina y liotironina en una proporción de 4:1, similares a las proporciones encontradas en preparados de tiroides desecado.
Usos Terapéuticos de la Hormona Tiroidea
- Hipotiroidismo: La levotiroxina es el tratamiento preferido debido a su potencia constante y larga duración de acción. El objetivo es normalizar la TSH sérica o la T4 libre y aliviar síntomas.
- Cáncer de Tiroides: Se utiliza levotiroxina para suprimir la TSH y reducir el riesgo de recurrencia del cáncer.
- Nódulos Tiroideos: No se recomienda el uso general de levotiroxina para suprimir nódulos tiroideos en individuos eutiroideos.
Efectos Adversos y Interacciones
- Efectos Adversos: Generalmente asociados con dosis excesivas, similares a los síntomas del hipertiroidismo como la fibrilación auricular y el riesgo de osteoporosis.
- Interacciones: Diversos fármacos y condiciones pueden influir en las necesidades de dosificación de levotiroxina.
Investigación en Análogos de la Hormona Tiroidea
- Agonistas Específicos de TRβ: Se investigan para regular procesos dependientes de la hormona tiroidea sin causar efectos secundarios indeseables, como los efectos cardíacos.
- Ácido Triyodotiroacético (Tiratricol): Se investiga para tratar síndromes causados por deficiencias en transportadores de hormonas tiroideas, como el síndrome de Allan-Herndon-Dudley.
Fármacos Antitiroideos
- Tioureilenos (Tioamidas): Incluyen propiltiouracilo y metimazol. Actúan inhibiendo la peroxidasa tiroidea, lo que reduce la síntesis de hormonas tiroideas.
- Propiltiouracilo: Además de inhibir la síntesis de hormonas, bloquea la conversión periférica de T4 a T3, útil en casos graves de hipertiroidismo.
Inhibidores Iónicos
- Bloquean el transporte de yoduro hacia la glándula tiroides, reduciendo la síntesis de hormonas tiroideas.
Yodo y Yodo Radiactivo
- Yodo: En altas concentraciones, puede disminuir la liberación y síntesis de hormonas tiroideas (efecto Wolff-Chaikoff).
- Yodo Radiactivo (131I): Destruye el tejido tiroideo mediante radiación ionizante, utilizado en el tratamiento del hipertiroidismo y cáncer de tiroides.
Tratamiento Adyuvante
- Incluye medicamentos para manejar síntomas periféricos de la tirotoxicosis, como bloqueadores beta y bloqueadores de canales de calcio.
Aplicaciones Clínicas
- Hipertiroidismo: Los antitiroideos son el tratamiento inicial, seguido de yodo radiactivo o cirugía si es necesario.
- Cáncer de Tiroides: El yodo radiactivo se utiliza después de la tiroidectomía para eliminar el tejido tiroideo restante y tratar las metástasis.
- Hipotiroidismo Congénito y Durante el Embarazo: La levotiroxina es el tratamiento estándar, con ajustes de dosis según sea necesario.
Consideraciones Especiales
- Embarazo: El tratamiento del hipertiroidismo requiere precaución; el metimazol se prefiere en el segundo y tercer trimestre, mientras que el propiltiouracilo puede ser utilizado en el primer trimestre debido a preocupaciones sobre teratogenicidad.
- Cáncer de Tiroides: La preparación para el tratamiento con yodo radiactivo puede implicar la suspensión temporal de la terapia con hormona tiroidea o el uso de tirotropina alfa para estimular la captación de yodo.
Efectos Adversos y Precauciones
- Los antitiroideos pueden causar efectos adversos graves como agranulocitosis y hepatotoxicidad. La monitorización cuidadosa es esencial.
- La terapia con yodo radiactivo conlleva el riesgo de hipotiroidismo a largo plazo y requiere consideraciones especiales para evitar la exposición a radiaciones en embarazadas y niños.
Tratamientos Dirigidos en el Cáncer de Tiroides
Inhibidores de la Cinasa
- Los tratamientos modernos para el cáncer de tiroides incluyen inhibidores de la cinasa, específicamente diseñados para bloquear las vías de señalización que promueven el crecimiento del cáncer.
- La necesidad de dosificación de levotiroxina puede aumentar en pacientes tratados con inhibidores de la proteína tirosina cinasa.
Carcinomas Papilares y Foliculares
- La mayoría se tratan con cirugía, yodo radiactivo y levotiroxina.
- Para casos que progresan, se utilizan inhibidores de la cinasa, guiados idealmente por el perfil genético del tumor.
- Inhibidores específicos para mutaciones NTRK o RET incluyen larotrectinib, entrectinib, selpercatinib y pralsetinib.
- Lenvatinib y sorafenib, inhibidores de la multicinasa, se usan en ausencia de mutaciones NTRK o RET.
- Mutaciones de BRAF V600E pueden tratarse con vemurafenib o dabrafenib.
Cáncer de Tiroides Anaplásico
- Muy agresivo y tratado con cirugía, radioterapia y, idealmente, quimioterapia basada en el perfil genético del tumor.
- Dabrafenib más trametinib está aprobado para tumores con mutación BRAF V600E.
Carcinoma Medular de Tiroides (MTC)
- Originado en células parafoliculares, no responde al yodo radiactivo.
- La cirugía es el tratamiento de primera línea.
- MTC avanzados pueden tratarse con inhibidores selectivos de RET como selpercatinib o pralsetinib, o con inhibidores de la multicinasa como vandetanib y cabozantinib.
Consideraciones Especiales
- Mutaciones Genéticas: La elección del tratamiento puede depender del perfil genético del tumor, particularmente en carcinomas papilares, foliculares y medulares de tiroides.
- Supervivencia sin Progresión: Los inhibidores de la cinasa pueden prolongar la supervivencia sin progresión, aunque las respuestas completas son raras.
- Efectos Secundarios y Dosificación de Levotiroxina: Es crucial monitorizar las concentraciones séricas de TSH en pacientes tratados con estos fármacos debido a la potencial necesidad de ajustar la dosis de levotiroxina.
| Fármaco | Usos Terapéuticos | Farmacología Clínica y Recomendaciones |
|---|---|---|
| Preparados de Hormonas Tiroideas | ||
| Levotiroxina (T4) | Hipotiroidismo, Supresión de la TSH en cáncer de tiroides | T1/2 plasmática de 1 semana. Necesidad de aumento de dosis durante embarazo. Riesgo de osteoporosis y fibrilación auricular con tratamiento excesivo. |
| Liotironina (T3) | Inicio rápido de acción (coma mixedematoso), preparación para yodo radiactivo en cáncer de tiroides | T1/2 plasmática de 18 a 24 h. Requiere múltiples dosis diarias. Levotiroxina preferida para tratamiento a largo plazo. |
| Tiroides desecada y mezclas de T4 y T3 | Algunos pacientes prefieren estas mezclas a la levotiroxina sola | Proporción de casi 4:1 por peso de T4:T3. No hay pruebas de mayor eficacia sobre levotiroxina sola. |
| Antitiroideos | ||
| Metimazol | Reduce la producción de hormonas tiroideas | Larga T1/2 intratiroidea, dosificación una vez al día. No usar en el primer trimestre del embarazo. |
| Propiltiouracilo | Reduce producción de hormonas tiroideas y conversión de T4 a T3 | Preocupación por toxicidad hepática, especialmente en niños y embarazo. Indicado en tormenta tiroidea y primer trimestre del embarazo. |
| Perclorato | Mejora respuesta a tionamidas en enfermedad de Graves resistente | No disponible comercialmente; compuesto especial. |
| Solución de Lugol y SSKI | Reducción aguda de hormona tiroidea | Efecto de “escape” después de 7 a 10 días. Contraindicado en embarazo. |
| Yodo Radiactivo | ||
| 131I | Tratamiento permanente de enfermedad de Graves, nódulo tóxico, cáncer de tiroides | Provoca hipotiroidismo permanente. Contraindicado en embarazo. |
| Agonistas de la TSH Humana Recombinante | ||
| Tirotropina alfa | Preparación para ablación con yodo radiactivo en cáncer de tiroides | Facilita el tratamiento con yodo radiactivo sin suspender la levotiroxina. |
| Quimioterapia del Cáncer de Tiroides | ||
| Larotrectinib, Entrectinib | Tratamiento sistémico de cánceres de tiroides con mutaciones del gen de fusión NTRK | Mejor tolerados y más eficaces que inhibidores de la multicinasa con gen de fusión NTRK. |
| Selpercatinib, Pralsetinib | Tratamiento sistémico de cánceres de tiroides con mutaciones conductoras de RET | Mejor tolerados y más eficaces que inhibidores de la multicinasa con mutación estimulante de RET. |
| Vemurafenib, Dabrafenib | Tratamiento sistémico de cánceres de tiroides con mutación V600E del gen BRAF | Puede ser útil como tratamiento de rediferenciación para inducir la captación de yodo radiactivo. |
| Lenvatinib, Sorafenib | Tratamiento sistémico de cánceres de tiroides derivados de células foliculares sin tener en cuenta el estado de mutaciones conductoras | Lenvatinib puede ser más eficaz según datos existentes. Toxicidades comunes que pueden limitar uso. |
| Vandetanib, Cabozantinib | Tratamiento sistémico del cáncer medular de tiroides sin tener en cuenta el estado de mutaciones estimulantes | Inhiben múltiples cinasas, incluyendo receptores del factor de crecimiento del endotelio vascular y RET. |
| Trametinib, Selumetinib | Tratamiento de cánceres anaplásicos con mutación V600E del gen BRAF | Aprobado en combinación para inducir la captación de yodo radiactivo en cánceres de tiroides no ávidos de yodo. Eficacia de los inhibidores de MEK desconocida. |
BIBLIOGRAFÍA
- Abduljabbar, M. A., & Afifi, A. M. (2012). Congenital hypothyroidism. Journal of Pediatric Endocrinology & Metabolism, 25, 13-29. 10.1515/jpem.2011.408
- Alexander, E. K., & Larsen, P. R. (2002). High dose of 131I therapy for the treatment of hyperthyroidism caused by Graves’ disease. Journal of Clinical Endocrinology & Metabolism, 87, 1073-1077. https://doi.org/10.1210/jcem.87.3.8310
- Alexander, E. K., et al. (2017). 2017 guidelines of the American Thyroid Association for the Diagnosis and Management of Thyroid Disease During Pregnancy and the Postpartum. Thyroid, 27, 315-389. https://doi.org/10.1089/thy.2016.0457
- Angell, T. E., et al. (2015). Clinical features and hospital outcomes in thyroid storm: a retrospective cohort study. Journal of Clinical Endocrinology & Metabolism, 100, 451-459. https://doi.org/10.1210/jc.2014-3190
- Biondi, B., & Wartofsky, L. (2014). Treatment with thyroid hormone. Endocrine Reviews, 35, 433-512. https://doi.org/10.1210/er.2013-1083
- Brent, G. A. (2008). Clinical practice. Graves’ disease. New England Journal of Medicine, 358, 2594-2605. https://doi.org/10.1056/NEJMcp0801880
- Brent, G. A. (2012). Mechanisms of thyroid hormone action. Journal of Clinical Investigation, 122, 3035-3043. https://doi.org/10.1172/JCI60047
- Cabanillas, M. E., et al. (2019). Targeted therapy for advanced thyroid cancer: kinase inhibitors and beyond. Endocrine Reviews, 40, 1573-1604. https://doi.org/10.1210/er.2018-00275
- Celi, F. S., et al. (2011). Metabolic effects of liothyronine therapy in hypothyroidism: a randomized, double-blind, crossover trial of liothyronine versus levothyroxine. Journal of Clinical Endocrinology & Metabolism, 96, 3466-3474. https://doi.org/10.1210/jc.2011-1245
- Cherella, C. E., & Wassner, A. J. (2020). Update on congenital hypothyroidism. Current Opinion in Endocrinology, Diabetes, and Obesity, 27, 63-69. https://doi.org/10.1097/MED.0000000000000529
- Grais, I. M., & Sowers, J. R. (2014). Thyroid and the heart. American Journal of Medicine, 127, 691-698. https://doi.org/10.1016/j.amjmed.2014.03.009
- Groeneweg, S., et al. (2020). Thyroid hormone transporters. Endocrine Reviews, 41, bnz008. https://doi.org/10.1210/endrev/bnz008
- Gullo, D., et al. (2011). Levothyroxine monotherapy cannot guarantee euthyroidism in all athyreotic patients. PLoS One, 6, e22552. https://doi.org/10.1371/journal.pone.0022552
- Haugen, B. R., et al. (2016). 2015 American Thyroid Association management guidelines for adult patients with thyroid nodules and differentiated thyroid cancer: The American Thyroid Association Guidelines Task Force on Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid, 26, 1-133. https://doi.org/10.1089/thy.2015.0020
- Haugen, B. R., & Sherman, S. I. (2013). Evolving approaches to patients with advanced differentiated thyroid cancer. Endocrine Reviews, 34, 439-455. https://doi.org/10.1210/er.2012-1054
- Hones, G. S., et al. (2017). Noncanonical thyroid hormone signaling mediates cardiometabolic effects in vivo. Proceedings of the National Academy of Sciences of the United States of America, 114, E11323-E11332. https://doi.org/10.1073/pnas.1706801114
- Jentzen, W., et al. (2014). Assessment of lesion response in the initial radioiodine treatment of differentiated thyroid cancer using 124I PET imaging. Journal of Nuclear Medicine, 55, 1759-1765. https://doi.org/10.2967/jnumed.114.143347
- Jonklaas, J., et al. (2021). Evidence-based use of levothyroxine/liothyronine combinations in treating hypothyroidism: a consensus document. Thyroid, 31, 156-182. https://doi.org/10.1089/thy.2020.0333
- Jonklaas, J., et al. (2014). Guidelines for the treatment of hypothyroidism: prepared by the American Thyroid Association task force on thyroid hormone replacement. Thyroid, 24, 1670-1751. https://doi.org/10.1089/thy.2014.0028
- Kogai, T., & Brent, G. A. (2012). The sodium iodide symporter (NIS): regulation and approaches to targeting for cancer therapeutics. Pharmacology & Therapeutics, 135, 355-370. https://doi.org/10.1016/j.pharmthera.2012.05.007
- Marsili, A., et al. (2011). Physiological role and regulation of iodothyronine deiodinases: a 2011 update. Journal of Endocrinological Investigation, 34, 395-407. https://doi.org/10.3275/7572
- Mullur, R., et al. (2014). Thyroid hormone regulation of metabolism. Physiological Reviews, 94, 355-382. https://doi.org/10.1152/physrev.00030.2013
- Onigata, K., & Szinnai, G. (2014). Resistance to thyroid hormone. Endocrine Development, 26, 118-129. https://doi.org/10.1159/000363158
- Portulano, C., et al. (2014). The Na+/I− symporter (NIS): mechanism and medical impact. Endocrine Reviews, 35, 106-149. https://doi.org/10.1210/er.2013-1059
- Pramyothin, P., et al. (2011). Clinical problem-solving. A hidden solution. New England Journal of Medicine, 365, 2123-2127. https://doi.org/10.1056/NEJMcps1103642
- Public Health Committee of the American Thyroid Association, et al. (2006). Iodine supplementation for pregnancy and lactation-United States and Canada: recommendations of the American Thyroid Association. Thyroid, 16, 949-951. https://doi.org/10.1089/thy.2006.16.949
- Ross, D. S. (2011). Radioiodine therapy for hyperthyroidism. New England Journal of Medicine, 364, 542-550. https://doi.org/10.1056/NEJMct1007101
- Wojcicka, A., et al. (2013). Mechanisms of action of thyroid hormones in the skeleton. Biochimica et Biophysica Acta (BBA) – Molecular Basis of Disease, 1830, 3979-3986. https://doi.org/10.1016/j.bbadis.2012.08.013
- Zimmermann, M. B. (2009). Iodine deficiency. Endocrine Reviews, 30, 376-408. https://doi.org/10.1210/er.2009-0011
- Zucchi, R. (2020). Thyroid hormone analogues: an update. Thyroid, 30, 1099-1105. https://doi.org/10.1089/thy.2019.0460